🏆 আজকের ফ্রি বাংলা কুইজ খেলুন এবং Gift Voucher পুরস্কারের জেতার সুযোগ নিন।
Play Now
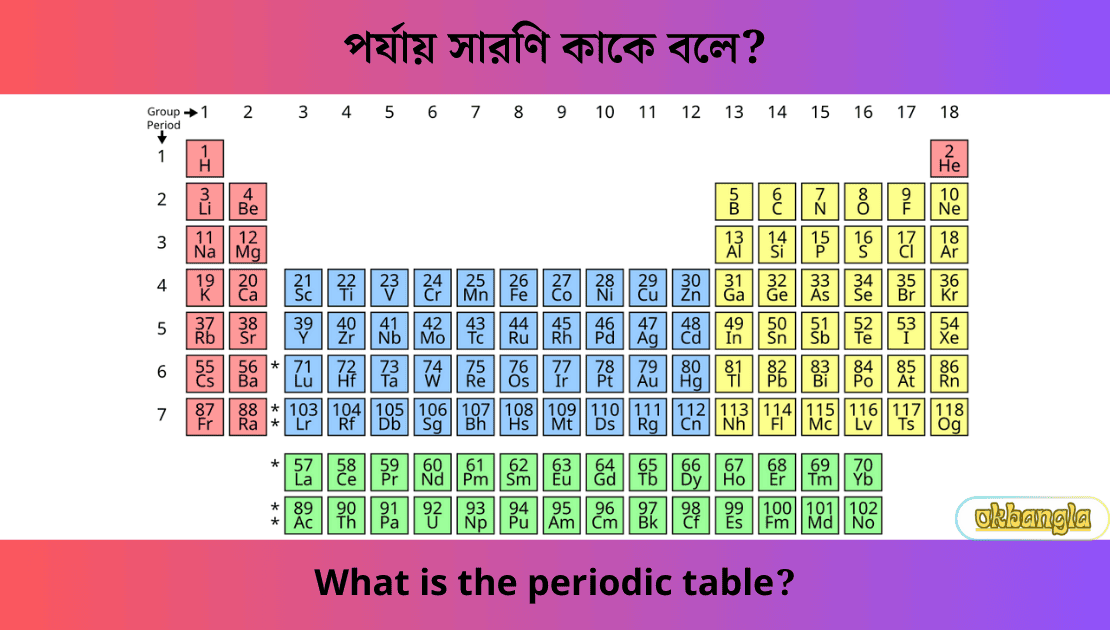
পর্যায় সারণী হল রসায়নের একটি অত্যন্ত গুরুত্বপূর্ণ সরঞ্জাম। এটি বিভিন্ন রাসায়নিক মৌলগুলিকে তাদের পারমাণবিক সংখ্যা এবং রাসায়নিক বৈশিষ্ট্য অনুযায়ী একটি নির্দিষ্ট ক্রমে সাজানোর এক প্রক্রিয়া। এই সারণীর সাহায্যে আমরা মৌলগুলির বিভিন্ন ধর্ম, তাদের মধ্যকার সম্পর্ক এবং নতুন মৌল আবিষ্কারের সম্ভাবনা সম্পর্কে অনেক কিছু জানতে পারি।
পর্যায় সারণি বলতে কি বোঝায়? What does the periodic table mean?
পর্যায় সারণি মৌলের পর্যায় সারণি নামেও পরিচিত, রসায়নের একটি অত্যন্ত গুরুত্বপূর্ণ উপাদান। এই সারণীতে রাসায়নিক মৌলগুলোকে সুবিন্যস্তভাবে সারি (“পর্যায়”) এবং কলাম (“গ্রুপ”) আকারে সাজানো থাকে। বিজ্ঞানের অঙ্গনে, বিশেষ করে রসায়ন এবং পদার্থবিদ্যায় এর ব্যাপক ব্যবহার লক্ষ্য করা যায়।
বিভিন্ন মৌলের ভৌত ও রাসায়নিক ধর্মের মধ্যে মিল-অমিল এবং সেই ধর্মগুলির ক্রম পরিবর্তন দেখানোর জন্য মৌলগুলিকে সাজিয়ে তৈরি করা সারণিকে আধুনিক পর্যায় সারণি বলে।
পর্যায় সারণীর ইতিহাস, History of the Periodic Table
পর্যায় সারণীর ইতিহাসের কিছু তথ্য হল:
- পর্যায় সারণি তৈরির প্রথম উদ্যোগ নেন ফরাসি ভূতাত্ত্বিক আলেকজান্দ্রে-এমিল-বেগুয়ের। তিনি ১৮৬২ সালে মৌলগুলির একটি পর্যায় সারণী প্রস্তাব করেন।
- রাশিয়ান রসায়নবিদ দিমিত্রি মেন্ডেলিভ ১৮৬৯ সালে সর্বপ্রথম সর্বজনীনভাবে গৃহীত পর্যায় সারণি তৈরি করেন। তিনি পারমাণবিক ভরের ওপর ভিত্তি করে রাসায়নিক বৈশিষ্ট্য সম্পর্কিত পর্যায় সারণি তৈরি করেন।
- মেন্ডেলিভের পর্যায় সারণি তৈরির জন্য তিনি একটি সাধারণ পর্যায় সূত্র আবিষ্কার করেন। এই সূত্র অনুযায়ী, মৌলসমূহের ভৌত ও রাসায়নিক ধর্ম তাদের পারমাণবিক ভর বৃদ্ধির সঙ্গে পর্যায় ক্রমে আবর্তিত হয়।
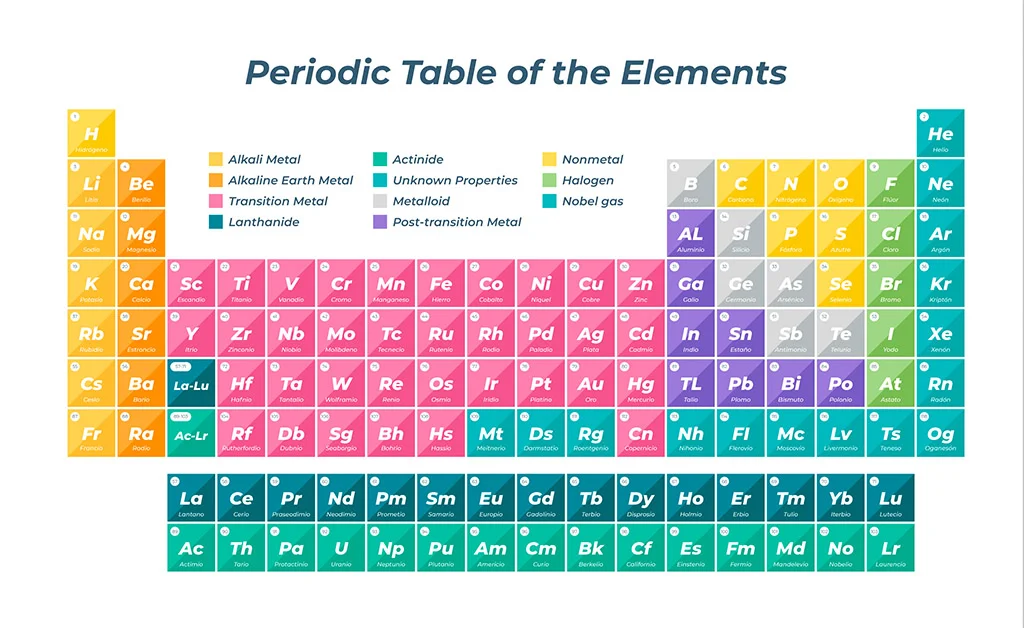
পর্যায় সারণীর গঠন, Structure of the periodic table :
পর্যায়: পর্যায় সারণীর অনুভূমিক সারিগুলিকে পর্যায় বলা হয়। একই পর্যায়ের মৌলগুলিতে সর্ববহিঃস্থ কক্ষপথে ইলেকট্রনের সংখ্যা সমান হয়।
গ্রুপ: পর্যায় সারণীর উল্লম্ব কলামগুলিকে গ্রুপ বলা হয়। একই গ্রুপের মৌলগুলিতে সর্ববহিঃস্থ কক্ষপথে ইলেকট্রনের সংখ্যা সমান হয় এবং তাদের রাসায়নিক বৈশিষ্ট্যও অনেকটা একই রকম হয়।
পর্যায় সারণীর ব্যবহার, Uses of the periodic table :
মৌলের বৈশিষ্ট্য নির্ণয়: কোনো মৌলের অবস্থান থেকে তার ধাতব বা অধাতব বৈশিষ্ট্য, আয়নীকরণ শক্তি, ইলেকট্রন আসক্তি ইত্যাদি বৈশিষ্ট্য অনুমান করা যায়।
রাসায়নিক বিক্রিয়া পূর্বাভাস: মৌলগুলির মধ্যকার বিক্রিয়ার ধরন এবং পণ্য সম্পর্কে ধারণা পাওয়া যায়।
নতুন মৌল আবিষ্কার: পর্যায় সারণীর ফাঁকা জায়গাগুলো থেকে নতুন মৌল আবিষ্কারের সম্ভাবনা সম্পর্কে ধারণা পাওয়া যায়।
পর্যায় সারণীর গুরুত্ব, Importance of Periodic Table :
পর্যায় সারণী রসায়ন, পদার্থবিজ্ঞান, জীববিজ্ঞানসহ বিভিন্ন বিজ্ঞান শাখায় ব্যবহৃত হয়। এটি নতুন উপাদান উদ্ভাবন, ওষুধ তৈরি, পরিবেশ সংরক্ষণ ইত্যাদি ক্ষেত্রে অত্যন্ত গুরুত্বপূর্ণ ভূমিকা পালন করে।
আধুনিক পর্যায় সারণীর জনক কে? Who is the father of the modern periodic table?
পর্যায় সারণী আবিষ্কারের কৃতিত্ব যায় রাশিয়ান রসায়নবিদ দিমিত্রি মেন্ডেলেভ-এর কাছে। তিনি ১৮৬৯ সালে সর্বপ্রথম সর্বজনীনভাবে গৃহীত পর্যায় সারণিটি প্রণয়ন করেন। তিনি পারমাণবিক ভরের ওপর ভিত্তি করে রাসায়নিক বৈশিষ্ট্য সম্পর্কিত পর্যায় সারণিটি তৈরি করেন।
কেন মেন্ডেলেভের কাজ এত গুরুত্বপূর্ণ? Why is Mendeleev’s work so important?
- মৌলের বৈশিষ্ট্যের পূর্বাভাস: মেন্ডেলিভের পর্যায় সারণি মৌলের বিভিন্ন বৈশিষ্ট্য, যেমন রাসায়নিক বিক্রিয়াশীলতা, ইলেকট্রন বিন্যাস ইত্যাদি সম্পর্কে পূর্বাভাস দেয়।
- নতুন মৌল আবিষ্কার: মেন্ডেলিভ তার পর্যায় সারণিতে কিছু ফাঁকা জায়গা রেখেছিলেন, যা পরে নতুন মৌল আবিষ্কারের পথ প্রশস্ত করে।
- রসায়নের ভিত্তি: পর্যায় সারণি আধুনিক রসায়নের অন্যতম গুরুত্বপূর্ণ সরঞ্জাম। এটি মৌলের মধ্যকার সম্পর্ক এবং তাদের বৈশিষ্ট্য সম্পর্কে আমাদের বোঝার জন্য অপরিহার্য।
পর্যায় সারণিতে ধাতু কয়টি ও কি কি? How many metals in the periodic table and what are they ?
পর্যায় সারণিতে সাধারণত ৮টি ধাতু থাকে এবং তাদের নাম হল:
- লিথিয়াম (Li)
- সবম (Be)
- নাইট্রোজেন (N)
- অক্সিজেন (O)
- ফ্লোরিন (F)
- নেন্ট্রন (Ne)
- সোডিয়াম (Na)
- ম্যাগনেসিয়াম (Mg)
পর্যায় সারণির বাম থেকে ডানে গেলে কি হয়? What happens when you go from left to right on the periodic table?
পর্যায় সারণীতে আমরা বাম থেকে ডানে গেলে প্রোটন সংখ্যা বৃদ্ধি পায়। পারমাণবিক ভর বৃদ্ধি পায় যখন আমরা Sg & Bh, Th & Pa, U & Np এবং Pu & Am মৌলগুলি বাদ দিয়ে পর্যায় সারণিতে বাম থেকে ডানে সরে যাই। পর্যায় সারণীতে বাম থেকে ডানে যাওয়ার সাথে সাথে বৈদ্যুতিক ঋণাত্মকতাও বৃদ্ধি পায়।
প্রথম পর্যায় সারণী কে আবিষ্কার করেন? Who discovered the first periodic table?
১৮৬৯ সালে রুশ বিজ্ঞানী দিমিত্রি মেন্ডেলিভের সকল মৌলের জন্য একটি সাধারণ পর্যায় সূত্র আবিষ্কার করেন, যা হলো- “মৌলসমূহের ভৌত ও রাসায়নিক ধর্ম তাদের পারমাণবিক ভর বৃদ্ধির সঙ্গে পর্যায় ক্রমে আবর্তিত হয়”। উক্ত সূত্রানুসারে তিনি ও জার্মান বিজ্ঞানী ইউলিয়ুস লোটার মাইয়ার মিলে আধুনিক পর্যায় সারণি প্রকাশ করেন।
আধুনিক পর্যায় সারণিতে কয়টি পর্যায় কয়টি শ্রেণি আছে? How many phases and how many classes are there in the modern periodic table?
আধুনিক পর্যায় সারণিতে 7টি পর্যায় এবং 18টি শ্রেণি রয়েছে।
জেনে রাখা ভালো :
- পর্যায় সারণীর অনুভূমিক সারিগুলিকে পর্যায় বলা হয়।
- পর্যায় সারণীর উল্লম্ব সারিগুলিকে শ্রেণী বলা হয়।
- পর্যায় সারণীর সমস্ত শ্রেণীর তাদের প্রথম মৌলের নামে নামকরণ করা হয়েছে।
- আধুনিক পর্যায় সারণীর দীর্ঘতম পর্যায় হলো 6 এবং 7 পর্যায়।
- এই দুটি পর্যায়েই 32টি মৌল রয়েছে।
- 6 পর্যায়ে ল্যান্থানাইড এবং 7 পর্যায়ে অ্যাক্টিনাইড মৌল রয়েছে।
রুশ বিজ্ঞানী দিমিত্রি মেন্ডেলিভ এবং জার্মান বিজ্ঞানী ইউলিয়ুস লোটার মাইয়ার মিলে আধুনিক পর্যায় সারণি প্রকাশ করেন। মেন্ডেলিভ মৌলগুলিকে তাদের ভৌত ও রাসায়নিক আচরণ অনুসারে শ্রেণী এবং সারিগুলিতে সংগঠিত করেছিলেন।
পর্যায় সারণির সবচেয়ে সক্রিয় মৌল কোনটি? Which is the most active element in the periodic table?
রাসায়নিকভাবে সবচেয়ে সক্রিয় মৌল হল ফ্লোরিন।
ফ্লোরিনের বৈশিষ্ট্য:
- ফ্লোরিনে 7টি ভ্যালেন্স ইলেকট্রন আছে।
- এটি প্রায় সব উপাদানের সঙ্গে বিক্রিয়া করে।
- উচ্চ তাপমাত্রা ও চাপে মহৎ গ্যাসের সঙ্গেও বিক্রিয়া করে।
- ফ্লোরিন সবচেয়ে ইলেক্ট্রোনেগেটিভ উপাদান।
পর্যায় সারণির সবচেয়ে ভারী অধাতু কোনটি? Which is the heaviest non-metal in the periodic table?
পর্যায় সারণির সবচেয়ে ভারী অধাতু হল আয়োডিন।
পর্যায় সারণির সবচেয়ে ভারী ধাতু কোনটি? Which is the heaviest metal in the periodic table?
সবচেয়ে ভারী প্রাকৃতিক মৌল হল ইউরেনিয়াম যার পারমাণবিক সংখ্যা 92 এবং পারমাণবিক ওজন 238 গ্রাম। 118-এর ধনাত্মক আধানযুক্ত প্রোটনের বিকর্ষণীয় শক্তি নিউক্লিয়াসের উপর প্রচণ্ড চাপ সৃষ্টি করে এবং এটি হালকা নিউক্লিয়াসে বিভক্ত হওয়ার আগে এক মিলিসেকেন্ডের নীচে কিছুটা স্থায়ী হয়।
পর্যায় সারণির সবচেয়ে ছোট মৌল কোনটি? Which is the smallest element in the periodic table?
পর্যায় সারণির বাম থেকে ডানে গ্রুপের পরিবর্তন হওয়ার ফলে পারমাণবিক ব্যাসার্ধ হ্রাস পায়। অন্যদিকে ওপর থেকে নিচে পর্যায়ের পরিবর্তনের ফলে পারমাণবিক ব্যাসার্ধ বৃদ্ধি পায়। পর্যায় সারণির সবচেয়ে ছোট পারমাণবিক ব্যাসার্ধের মৌল হলো হিলিয়াম He(2). আর সবচেয়ে বড় পারমাণবিক ব্যাসার্ধের মৌলটি হলো ফ্রান্সিয়াম Fr (87)।
পর্যায় সারণির সবচেয়ে বড় মৌলের নাম কি? What is the name of the largest element in the periodic table?
পর্যায় সারণির সবচেয়ে বড় পারমাণবিক ব্যাসার্ধের মৌল হল ফ্রান্সিয়াম (Fr)। এর পারমাণবিক সংখ্যা 87। অন্যদিকে, পর্যায় সারণির সবচেয়ে ছোট পারমাণবিক ব্যাসার্ধের মৌল হল হিলিয়াম (He)। এর পারমাণবিক সংখ্যা 2।
পর্যায় সারণীতে বাম থেকে ডানে গ্রুপের পরিবর্তন হওয়ার ফলে পারমাণবিক ব্যাসার্ধ কমে যায়। অন্যদিকে, ওপর থেকে নিচে পর্যায়ের পরিবর্তন হওয়ার ফলে পারমাণবিক ব্যাসার্ধ বাড়ে।
পর্যায় সারণিতে ধাতু ও অধাতু কয়টি ও কি কি? / আধুনিক পর্যায় সারণিতে কয়টি ধাতু আছে? How many metals are there in the modern periodic table?
আধুনিক পর্যায় সারণিতে মোট 91টি ধাতু আছে। আধুনিক পর্যায় সারণিতে মোট 118টি মৌল রয়েছে, যার মধ্যে 7টি ধাতুকল্প এবং 20টি অধাতু আছে।
পর্যায় সারণির সঙ্গে জড়িত কিছু তথ্য:
- পর্যায় সারণিতে মোট মৌলের সংখ্যা 118টি।
- এর মধ্যে 91টি ধাতু, 7টি ধাতুকল্প, এবং 20টি অধাতু রয়েছে।
- পর্যায় সারণির সবচেয়ে ভারী প্রাকৃতিক মৌল হল ইউরেনিয়াম।
- পর্যায় সারণির সবচেয়ে শক্ত ধাতু হল টাংস্টেন।
- পর্যায় সারণির সবচেয়ে ভারী উপাদান হল অজানা উপাদান (বা ট্রানস্যাক্টিনাইড)।
- বিজ্ঞানের মতে, বিশ্বের সবচেয়ে ভারী পদার্থ হল ওগানেসন।
পর্যায় সারণি মনে রাখার কৌশল, Techniques for memorizing the periodic table :
পর্যায় সারণির এতোগুলো মৌলের নাম সহজে মনে রাখা সম্ভব না। কিন্তু বিদ্যালয়ের পরীক্ষার জন্য হোক বা অন্য বিভিন্ন কাজে, পর্যায় সারণি -এর মৌলগুলোর নাম ও পর্যায় সারণিতে এদের স্থান মনে রাখা অত্যন্ত জরুরি। তবে কিছু কৌশল আছে যার মাধ্যমে আমরা সহজেই মৌলগুলোর নাম মনে রাখতে পারি, যেমন ছন্দের মাধ্যমে মৌলগুলোর নাম মনে রাখা সহজ। এখানে কিছু ছন্দের মাধ্যমে আমরা পর্যায় সারণির মৌলগুলোর নাম মনে রাখার উপায় বলে দেবো :
গ্রুপ ১ – হায় – H – হাইড্রোজেন
লি – Li – লিথিয়াম
না – Na – সোডিয়াম
কে – K – পটাশিয়াম
রুবি – Rb – রুবিডিয়াম
ছেঁচে – Cs – সিজিয়াম
ফেলেছে – Fr – ফ্রানসিয়ামগ্রুপ ২ – বিরিয়ানি – Be – বেরিলিয়াম
মোগলাই – Mg – ম্যাগনেসিয়াম
কাবাব – Ca – ক্যালসিয়াম
সরিয়ে – Sr – স্ট্রোনসিয়াম
বাটিতে – Ba – বেরিয়াম
রাখো – Ra – রেডিয়ামগ্রুপ ১৩ – বো – B – বোরন
য়াল – Al – অ্যালুমিনিয়াম
গেলো – Ga – গ্যালিয়াম
ইন্ডিয়া – In – ইনডিয়াম
তেও যাই – Ti – থ্যালিয়ামগ্রুপ ১৪ – কাল – C – কার্বন
সিলেট – Si – সিলিকন
গেলে – Ge – জারমেনিয়াম
স্বর্ন – Sn – টিন
পাবো – Pb – লেডগ্রুপ ১৫ – নানা – N – নাইট্রোজেন
পাটেকার – P – ফসফরাস
আসলো – As – আর্সেনিক
সব – Sb – অ্যান্টিমনি
বিলিয়ে – Bi – বিসমাথগ্রুপ ১৬ – ও – O – অক্সিজেন
এস – S – সালফার
এস সি – Se – সেলেনিয়াম
তে – Te – টেলুরিয়াম
পড়ে – Po – পোলোনিয়ামগ্রুপ ১৭ – ফকিরা – F – ফ্লোরিন
কালু – Cl – ক্লোরিন
বরিসাল থেকে – Br – ব্রোমিন
ইস্টিমারে – I – আয়োডিন
আসতেসে – At – অ্যাস্টাটিনগ্রুপ ১৮ – হিলি – He – হিলিয়াম
নিয়ন্তা – Ne – নিয়ন
আর – Ar – আর্গন
কিশোর – Kr – ক্রিপ্টন
যাবে – Xe – জেনন
রংপুর – Rn – রেডনপর্যায় ৩ – না – Na – সোডিয়াম
মাযে – Mg – ম্যাগনেসিয়াম
এসে – Al – অ্যালুমিনিয়াম
সিজদায় – Si – সিলিকন
পড়ে – P – ফসফরাস
সবাই – S – সালফার
কালেমা – Cl – ক্লোরিন
আওড়ায় – Ar – আর্গনপর্যায় সারণি মনে রাখার এই কৌশলটি ব্যবহার করে ছন্দের সাথে পড়লে সহজেই মৌলগুলোর নাম ও কোনটি কোন পর্যায়ের এবং কোন গ্রুপে আছে তা বলতে পারবো।
শেষ কথা, Conclusion :
আজকের এই প্রতিবেদন থেকে আপনারা পর্যায় সারণী সম্পর্কে বিস্তারিত জানতে পেরেছেন। আশা করি উল্লেখ করা তথ্যগুলো আপনাদের বিভিন্ন সময়ে সহায়ক হবে। আজকের এই প্রতিবেদন অবশ্যই আপনাদের পরিবারে থাকা শিক্ষার্থীদের সাথে শেয়ার করে নেবেন।